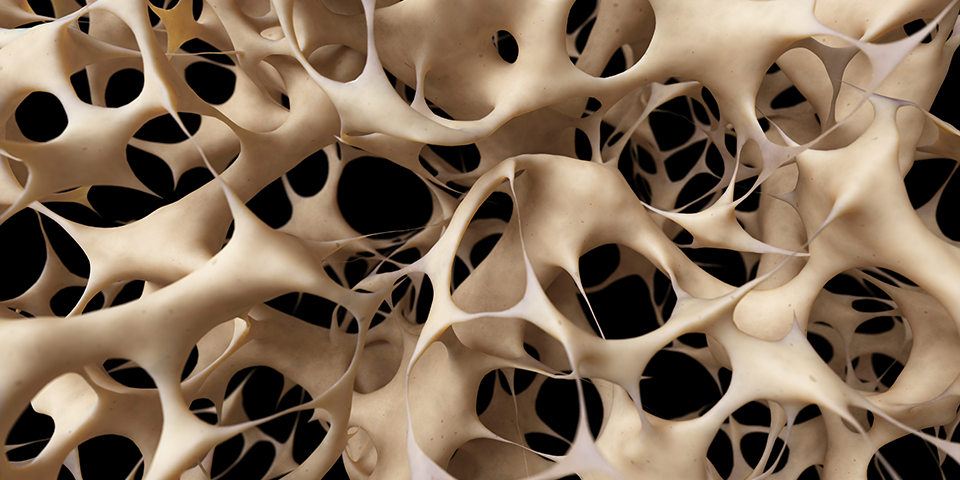
La osteonecrosis, también conocida como necrosis aséptica, necrosis avascular (AVN), necrosis atraumática y necrosis isquémica, es un proceso patológico que se ha asociado con numerosas afecciones e intervenciones terapéuticas. En los pacientes en los que hay daño directo a la vasculatura ósea (p. Ej., Fractura del cuello femoral) o lesión directa de elementos óseos o de la médula ósea (p. Ej., Lesión por radiación, disbarismo o enfermedad de Caisson), la causa es claramente identificable. Sin embargo, en muchos pacientes, los mecanismos por los cuales se desarrolla este trastorno no se comprenden completamente.
El daño de la vasculatura ósea, que conduce a la muerte de las células óseas y de la médula (infarto de médula ósea), y la falla mecánica final parece ser común en la mayoría de las etiologías propuestas. El proceso suele ser progresivo, lo que resulta en la destrucción de las articulaciones en unos pocos meses o dos años en la mayoría de los pacientes.
 Una variedad de factores traumáticos y atraumáticos contribuyen a la etiología de la osteonecrosis. Se ha establecido un papel etiológico definitivo para algunos de estos factores, basado en estudios de cohortes longitudinales o metanálisis, pero no para la mayoría, que se consideran factores de riesgo asociados. El uso de glucocorticoides y el consumo excesivo de alcohol están asociados con más del 80 por ciento de los casos atraumáticos.
Una variedad de factores traumáticos y atraumáticos contribuyen a la etiología de la osteonecrosis. Se ha establecido un papel etiológico definitivo para algunos de estos factores, basado en estudios de cohortes longitudinales o metanálisis, pero no para la mayoría, que se consideran factores de riesgo asociados. El uso de glucocorticoides y el consumo excesivo de alcohol están asociados con más del 80 por ciento de los casos atraumáticos.
La patogenia de la osteonecrosis es un área de controversia. La mayoría de los expertos creen que es el resultado de los efectos combinados de la predisposición genética, los factores metabólicos y los factores locales que afectan el suministro de sangre, como el daño vascular, el aumento de la presión intraósea y el estrés mecánico. Las primeras etapas de la historia natural no están claras, ya que estas etapas son en gran medida asintomáticas y en el paciente no se presenta hasta más tarde. Generalmente se acepta que hay una interrupción de la circulación sanguínea dentro del hueso; posteriormente, el área adyacente se vuelve hiperémica, lo que resulta en desmineralización, adelgazamiento trabecular y, más tarde, colapso.
El hallazgo histopatológico del infarto de médula ósea se ha observado en muestras de médula de pacientes con algunos de los mismos trastornos que causan osteonecrosis clínicamente aparente, pero los trastornos neoplásicos, particularmente los tumores malignos hematológicos y linfoides y el cáncer metastásico con coagulopatía asociada, son otras posibles etiologías. Las causas del infarto de médula ósea (necrosis de médula ósea) se discuten en otra parte.Los pacientes tratados con altas dosis prolongadas de glucocorticoides parecen tener el mayor riesgo de desarrollar osteonecrosis; sin embargo, estos pacientes a menudo tienen muchos otros factores de riesgo. Incluso los pacientes que reciben reemplazo fisiológico crónico de glucocorticoides por insuficiencia suprarrenal pueden desarrollar osteonecrosis (2.4 por ciento según un informe). Sin embargo, la osteonecrosis generalmente no resulta del uso a corto plazo de estos medicamentos. En informes anecdóticos anteriores que sugerían una asociación, también estaban presentes múltiples factores de riesgo adicionales, lo que sugiere que era muy poco probable que estas dosis bajas condujeran a la enfermedad.
El consumo excesivo de alcohol y el desarrollo de osteonecrosis se han relacionado durante mucho tiempo; la embolia grasa, la hipertrofia de los adipocitos, la estasis venosa y el aumento de los niveles de cortisol han sido implicados como factores etiológicos. Mientras que solo un pequeño porcentaje de alcohólicos desarrolla osteonecrosis, el alcohol se ha considerado un factor de riesgo asociado en hasta el 31 por ciento de los pacientes con osteonecrosis evaluados.
El diagnóstico precoz de la osteonecrosis puede brindar la oportunidad de prevenir el colapso y, en última instancia, la necesidad de un reemplazo articular. Sin embargo, la mayoría de los pacientes se presentan tarde en el curso de la enfermedad. Por lo tanto, un alto índice de sospecha es necesario para aquellos con factores de riesgo conocidos o probables, particularmente el uso de dosis altas de corticosteroides.
Los hallazgos físicos son en gran medida inespecíficos. Los pacientes con enfermedad de la cadera pueden tener dolor y, eventualmente, limitaciones del rango de movimiento, particularmente con rotación interna forzada y abducción. Una cojera puede estar presente tarde en el curso de la enfermedad de las extremidades inferiores.
Un diagnóstico clínico se realiza de manera apropiada en un paciente sintomático cuando los hallazgos de imágenes por resonancia magnética (MRI) o de imágenes radiográficas son compatibles con esta enfermedad y cuando otras causas de dolor y anormalidades óseas son poco probables o han sido excluidas por las pruebas apropiadas. La resonancia magnética sin un agente de contraste sigue siendo el "estándar de oro" para el diagnóstico en pacientes sintomáticos y asintomáticos, especialmente en la enfermedad en estadio temprano
Los sistemas de clasificación para la estadificación de la osteonecrosis se han basado en hallazgos patológicos o en imágenes.
Estadificación patológica: los hallazgos patológicos son similares en todos los casos de osteonecrosis, independientemente de la etiología. A principios de la década de 1970 se propuso un esquema de clasificación que es útil para fines patológicos, pero no se correlaciona con la etapa radiográfica de la enfermedad o con los síntomas:
Cualquiera o todos los tipos patológicos se pueden ver en una muestra dependiendo del muestreo.
Estadificación clínica: se han desarrollado numerosos sistemas de estadificación para la osteonecrosis de la cabeza femoral. Las nuevas modalidades de imagen, como la tomografía computarizada (TC) y la resonancia magnética (MRI), y la necesidad de cuantificar la participación han llevado a estas revisiones. Además, también se reconoció la importancia del tamaño y la extensión de la lesión en el pronóstico de varios tratamientos. El sistema de estadificación de la Asociación de Investigación de Circulación Ósea (ARCO) se desarrolló en un intento de aportar uniformidad a los ensayos clínicos de estrategias de tratamiento. Este sistema de estadificación se ha modificado posteriormente para incluir una etapa 3 temprana y tardía.
